
Kinderen en mensen met ovotesticulair dsd hebben ovotestes. Dat wil zeggen dat ze ofwel 1 eierstok en 1 teelbal hebben, ofwel dat ze geslachtsklieren hebben waarin zowel eierstokweefsel als teelbalweefsel aanwezig is.
Ongeveer 1/3 personen met ovotesticular dsd heeft 1 eierstok en 1 teelbal.
Bij 2/3 personen met ovotesticulair dsd is er gecombineerd eierstok-en teelbalweefsel in dezelfde geslachtsklier.
De geslachtsklieren liggen vaak in de buikholte of lieskanaal. Soms kan de teelbal ook zijn ingedaald.
Mensen met ovostesticulair dsd hebben meestal twee X chromosomen (46,XX).
Sommige mensen met ovotesticulair dsd hebben een X en Y chromosoom (46, XY) en andere mensen twee X chromosomen in sommige lichaamscellen en een X en Y chromosoom in andere cellen (46, XX/46, XY).
1. WAT IS OVOTESTICULAIR DSD EN HOE VAAK KOMT HET VOOR?

Afhankelijk van hoeveel androgenen net worden aangemaakt door de teelbal of ovotestes en hoe het lichaam erop reageert, is er een heel spectrum mogelijk hoe het genitale uiterlijk eruit ziet. Bij sommige pasgeborenen met ovotesticulair is het op basis van het genitale uiterlijk voor een niet-getrainde arts niet onmiddellijk duidelijk of het om een jongen of meisje gaat. Artsen gebruiken soms de term 'ambigu genitaal' hiervoor.
Het is bijvoorbeeld niet duidelijk of het om een grote clitoris of kleine penis gaat, of om schaamlippen die (deels) vergroeid zijn, of een balzak die gespleten is. Het gaat hier enkel om hoe we iets moeten noemen, want het gaat bij iedereen, jongens/mannen en meisjes/vrouwen, eigenlijk altijd over hetzelfde weefsel (clitorophallus, labioscrotale plooien met bepaalde dimensies). Elke poging om duidelijke clitoris-of penis grenzen te bepalen (of schaamlippen of balzak-grenzen) is trouwens altijd subjectief, en hangt af van hoe er net gemeten wordt.
'Ambigu' is daarom zelf dus een zeer ambigue term om in deze context te gebruiken.

Omdat ovotestes zowel teelbal -als eierstokweefsel bevatten, kunnen ze zowel een beetje androgenen als oestrogenen produceren in de puberteit. De lichaamseffecten die die hormonen typisch zoal veroorzaken in de puberteit, zoals acne en lichaamsbeharing (oksel-of schaamhaar) en borstontwikkeling en vet rond heupen, variëren van persoon tot persoon met ovotesticulair dsd.
Ovotesticulair dsd komt voor bij ongeveer 1-100.000 personen, en zowel bij meisjes als bij jongens. Hoe meer androgeen signalen werden geproduceerd en opgepikt door het lichaam en de hersenen, hoe groter de kans dat kinderen met ovotesticulair zich beter zullen voelen als jongen en man.
2. WAT VEROORZAAKT OVOTESTICULAIR DSD?
Bij 10% van de mensen met XX chromosomen en ovotestes, kan er een translocatie van het SRY gen worden gevonden. Het SRY gen speelt een rol bij de ontwikkeling van teelballen.
Veranderingen in andere genen, zoals SOX9, RSPO1 en DMRT1 zijn ook beschreven.
Bij de overgrote meerderheid (ongeveer 90%) van de personen is echter geen genetische oorzaak gekend.
Ook bij mensen met ovotestes en XY chromosomen of een mozaiek patroon (46XX/46, XY) is er geen gekende genetische oorzaak.
Hoewel ovotesticulair dsd is aangeboren, is het net erfelijk. De oorzaak is meestal een spontane genetische verandering, die NIET is doorgegeven via de biologische ouder(s).

> Lees hier meer over wat af te wegen bij genetische testen
3. ONDERZOEK
Ovotesticulair dsd komt zowel bij meisjes als jongens voor en wordt vaak bij de geboorte vastgesteld, omwille van een genitaal verschil. Zeer milde verschillen in het genitale uiterlijk, zoals een grotere clitoris of hypospadie, die niet altijd meteen bij de geboorte worden vastgesteld kunnen ook op pas op kinderleeftijd (of later) tot een diagnose van ovotesticulair dsd leiden.
Soms geeft een liesbreuk (inguinale hernia) op baby-of kinderleeftijd aanleiding tot verder diagnostisch onderzoek.
Een liesbreuk is uitstulping van het buikvlies door een zwakkere plek of opening in de buikwand.
Bij een liesbreuk kunnen dan ook gonaden/geslachtsklieren tevoorschijn komen. Als die gonaden verder worden onderzocht (via een biopt), kan duidelijk worden dat ze (wat) testisweefsel, en eierstokweefsel bevatten.
Soms komt ovotesticulair dsd pas tijdens de adolescentie aan het licht, omdat (sommige) meisjes met ovotesticulair dsd hun maandstonden niet krijgen, of als er meer haargroei of groei van de clitoris komt door aanmaak van testosteron door het testisweefsel in de puberteit.
Enkele bijkomende onderzoeken, zoals chromosomenonderzoek, hormonaal onderzoek en stimulatietesten, echografisch onderzoek van inwendige reproductieve organen, en eventueel verder genetisch onderzoek kunnen worden ingezet om de specifieke biologische achtergrond verder in kaart te brengen.
-
Chromosomen zijn vaak 46, XX, maar kunnen ook 46, XY en 46, XX/46, XY zijn
-
Hormonaal onderzoek bij mensen met ovotesticulair dsd laat zien dat de testosteron en oestrogeen concentraties vaak laag zijn.
-
Zowel mannen als vrouwen met ovotesticulair dsd hebben gonaden die testiculair weefsel en/of eierstokweefsel bevatten, maar het is niet duidelijk of ze ook sperma/eicellen produceren. De gonaden zitten vaak in het lieskanaal of buikholte en zijn niet verder ingedaald. Deze gonaden zullen vaak medisch worden opgevolgd.
-
Afhankelijk van hoeveel hormoon AMH de gonaden hebben aangemaakt, zullen er een kleine baarmoeder en eileider zijn. Sommige vrouwen met ovotesticulair dsd kunnen hun maandstonden krijgen. Mannen met ovotesticulair dsd hebben vaak geen baarmoeder. Er kan een kleine prostaat en zaadleider zijn.
-
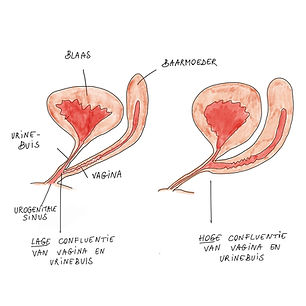
De vagina kan bij sommige vrouwen met ovotesticulair dsd wat kleiner/korter zijn dan bij vrouwen zonder ovotesticulair dsd Soms komen ook het vaginale kanaal en de urinebuis samen (urogenitale sinus, of confluentie van de vagina en urinebuis). Ook dit wordt vaak medisch opgevolgd, om na te gaan of er geen urinewegproblemen kunnen optreden.
-
Bij mannen met ovotesticulair dsd is er vaak sprake van een kleinere penis en hypospadie. Bij hypospadie mondt de urinebuis niet uit aan de top van de penis maar ergens op de schacht of onderaan. Ook hier is een heel spectrum mogelijk.

4. OPVOLGING OVOTESTICULAIR DSD
1. GENITALE UITERLIJK IN DE KINDERTIJD
Is een verschil in het genitale uiterlijk reden tot medische bezorgdheid?
Een verschil in het genitale uiterlijk, zoals een grotere clitoris, heeft meestal geen medische gevolgen, maar kan in sommige gevallen wel wijzen op andere hormoontekorten, zoals bij bijnierschorshyperplasie het geval is.
Is een ingreep aan het genitale uiterlijk medisch noodzakelijk ?
Indien urine het lichaam niet kan verlaten, is dat wel een medisch noodzakelijke reden om in te grijpen. Lichamelijk onderzoek, via een vagino-of uroscopie, kan dat uitwijzen.
In de meeste gevallen is een operatie die bedoeld is om het ambigu genitaal typisch 'vrouwelijker' of 'mannelijker' te maken, niet medisch noodzakelijk.
Het kan hierbij onder meer gaan om een
-
operatie om de clitoris te verkleinen
-
operatie om de (deels) vergroeide schaamlippen van elkaar te scheiden of scrotumhelften bij elkaar te brengen
-
operatie om de urinebuis aan de top van de penis te laten uitmonden
-
operatie aan de vagina en urinebuis (urogenitale sinus) op jonge leeftijd, om sommige seksuele activiteiten te vergemakkelijken op latere leeftijd
Omdat het niet-medisch noodzakelijke ingreep gaat is, is er steeds voldoende tijd om hier een beslissing over te nemen, en te overleggen met beroepsmensen en andere personen die een gelijkaardige ervaring hebben.
Wat zijn de mogelijke gevolgen van het al dan niet hebben van een operatie aan het genitale uiterlijk op jonge leeftijd?
Onderzoek wijst op specifieke gevolgen voor elk type beslissing, en daarom is het ook nuttig om te weten over welke ingreep het precies gaat.
Er bestaat geen onderzoek dat gevolgen van ingrijpen op jonge leeftijd vergelijkt met de gevolgen van niet-ingrijpen. Het meeste onderzoek is gebeurd bij mensen die op jonge leeftijd zijn geopereerd. Onderzoek bij kinderen die niet zijn geopereerd, staat in zijn kinderschoenen.
Uit beide types onderzoeken kunnen we volgende algemene gevolgen afleiden, voor kinderen en hun ouder(s) en hun onderlinge (hechtings)band. We staan uitgebreider stil bij de effecten op de persoon zelf, omdat die de centrale persoon is. Toch is ook onderzoek bij ouders van belang om te begrijpen waar ingrijpen al dat niet een rol bij speelt (Liao & Simmonds, 2013; Lundberg, 2017).
Twijfel je over een operatie voor je kind? Stel je dan ook deze vragen.

1
Gevolgen voor de ouder-kind relatie

2
Gevolgen voor het kind zelf

3
Gevolgen voor de ouders
2. GENITALE BEHANDELING OP LATERE LEEFTIJD (LATE ADOLESCENTIE/VOLWASSENHEID)
Vagina
Bij sommige -niet alle - meisjes/vrouwen met ovotesticulair dsd is er een kleinere/kortere vagina (en soms ook een urogenitale sinus). Dit kan (maar hoeft niet per se) problemen te geven bij sommige seksuele activiteiten. Seks en seksueel plezier betekenen verschillende dingen voor verschillende mensen. Vrouwen met ovotesticulair dsd hebben een clitoris die -net zoals bij vrouwen zonder ovotesticulair dsd - zeer orgasmegevoelig is (en gevoeliger is dan de vagina).
Er bestaan heel wat technieken om de vagina iets dieper te maken, moesten meisjes/vrouwen met ovotesticulair dsd dit zelf willen. Deze behandelingen worden nooit in de kindertijd uitgevoerd, omdat meisjes en vrouwen zelf actief moeten betrokken zijn bij deze behandelingen voor het welslagen ervan. Vaak worden de behandelingen pas vanaf de leeftijd van 16-17 jaar opgestart.
Omdat er heel wat risico's verbonden zijn aan een operatieve behandeling, wordt vaak eerst een niet-operatieve dilatatie behandeling voorgesteld. Die kan zeer succesvol zijn. Als zij niet de gewenste resultaten oplevert, kan nog steeds worden overgegaan op een operatie.

> Lees hier meer over vaginale behandelingen
Penis
Bij jongens/mannen met ovotesticulair dsd is er vaak een kleinere/kortere penis.
Testosterontherapie (in de kindertijd) of later heeft vaak geen blijvende invloed op de groei van de penis bij jongens/mannen geboren met een kleinere penis (Callens et al, 2013). Ook een operatie uitgevoerd voor hypospadie (in de kindertijd of later) zal de lengte van de penis niet echt beïnvloeden.
De meeste mannen met een kleine penis die deelgenomen hebben aan onderzoek, hebben een operatie gehad aan hun penis in de kindertijd, en zij zijn vaak minder tevreden over hun genitale uiterlijk. Ongeveer 60% van de mannen zegt dat dit negatieve genitale zelfbeeld ook een invloed heeft gehad op hun (seksueel) zelfvertrouwen, vooral als mannen er ook kwetsende commentaren op hebben gekregen (Callens, 2014).
Voor sommige mannen (ongeveer 30%) blijft de lengte van de penis moeilijk, ook na een operatie. Die lengte van de penis kan (maar hoeft niet per se) problemen te geven bij sommige seksuele activiteiten. Seks en seksueel plezier betekenen verschillende dingen voor verschillende mensen.
Op latere leeftijd kunnen mannen daarom zelf kiezen voor een falloplastie, die de lengte van de penis enigzins kan doen toenemen (ook al zijn na een operatie sommige mannen nog steeds niet tevreden). Een falloplastie is een erg zware operatie, en ook nog een experimentele behandeling bij mannen die geboren zijn met een kleine penis.

> Lees hier meer over falloplastie
3. GONADEN
Er wordt vanuit gegaan dat de gonaden of geslachtsklieren best medisch opgevolgd worden, omdat er een kans bestaat op tumorvorming in die gonaden als ze immature kiemcellen bevatten. Immature kiemcellen zijn kiemcellen die niet verder zijn uitgegroeid tot zaad-of eicellen.
Bij mensen met twee X chromosomen is er geen verhoogd tumorrisico; bij mensen met 46,XY of 46, XX/46, XY is het risico laag (2.6%). Het is onduidelijk of dit risico nog stijgt met de leeftijd.
Wat betekent dit risico echt?
Stel dat een dokter aangeeft dat er een risico van 3% is op tumorvorming van de gonaden. Dat betekent concreet dat bij ongeveer 3 op 100 mensen lokale celdeling (goed-of kwaadaardig) kan optreden. Het is niet geweten of die celdeling ook altijd tot invasieve tumorvorming leidt. Omgekeerd wil datzelfde cijfer ook zeggen dat er bij 97 op 100 mensen kans bestaat dat er géén ongewenste celdeling of tumorvorming ontstaat. Vroeger werden gonaden vaak bij iedereen preventief weggenomen. Nu komt men daar, in medische richtlijnen, op terug, en worden uitgebreider onderzoeken gedaan.
Ter vergelijking: Vrouwen hebben in hun leven ongeveer 1 op 7 kans dat ze ooit borstkanker krijgen. Niet bij alle 7 vrouwen zullen artsen voorstellen om de borsten preventief te verwijderen om die kans te doen dalen.
> Lees hier meer over hoe ons brein risico's inschat
Voor de waardering van risico’s bestaan geen objectieve maatstaven. Daarom is het onjuist om te veel te vertrouwen op het oordeel van deskundigen alleen. Deskundigen kunnen slechts het materiaal aanleveren op basis waarvan keuzes gemaakt worden. Deze keuzes moeten uiteindelijk door de persoon zelf aangevoeld en gewogen worden.
Welke factoren spelen nog een rol? (voor een overzicht, klik hier)
Gonaden die in de buikholte liggen hebben een verondersteld hoger risico op tumorvorming dan gonaden gelegen in de lies (of lager). Zowel in de buikholte als in de lies kunnen gonaden via echografisch onderzoek opgevolgd worden, al is dat niet altijd even evident. Kwaadaardige afwijkingen kunnen op echo en MRI worden gemist. Er zijn ook momenteel geen 'biomarkers' (signalen in het lichaam) die tot vroege(re) detectie van tumoren kunnen leiden.
Artsen kunnen een gonadale biopsie voorstellen als een optie om gonaden die moeilijk op echo/MRI te volgen zijn, verder te onderzoeken. Bij een biopsie wordt een klein deel van het weefsel van de gonade(n) weggesneden via een kijkoperatie en (microscopisch) onderzocht. Deze kijkoperatie houdt ook eigen risico's in, zoals schade aan de gonade(n) en eventueel verlies ervan.
WELKE OPTIES BESTAAN DAN VOOR MANAGEMENT VAN DE GESLACHTSKLIEREN?
Op basis van de verzamelde informatie rond het risico, zal het multidisciplinair team een advies uitbrengen:
1. gonadectomie (letterlijk het wegsnijden van de gonaden) op korte termijn;
2. puberteit afwachten, zo nodig tussentijds geslachtsklieren opvolgen en daarna gonadectomie;
3. gonaden blijven ter plekke en worden tussentijds opgevolgd
Het is belangrijk om deze evaluatie te laten doen door zorgverleners met expertise. Hier kan je nagaan of jouw zorgverlener voldoende ervaring heeft.
Meisjes/vrouwen
In medische richtlijnen wordt bij deze groep vaak geen gonadectomie voorgesteld in de kindertijd, zeker het als het genitale uiterlijk bij de geboorte niet ambigu was. Bij meisjes met een ambigu genitaal uiterlijk bij de geboorte, stelt men wel vaak wel een gonadectomie op kinderleeftijd voor, omdat vanaf de puberteit de gonaden soms testosteron beginnen produceren. Er kunnen dan enkele lichaamsveranderingen optreden (meer lichaamsbeharing, groei clitoris, wat verlaging van de stem). Niet alle vrouwen hebben hier last van. Indien dat wel is, kan op aangeven van de vrouw zelf, de gonaden worden weggenomen. Het is moeilijker om een deeltje van de gonade weg te nemen als er zowel eierstok-als teelbalweefsel in dezelfde gonade aanwezig zijn. Die delen lopen vaak ook in mekaar over, en zijn moeilijk van elkaar te scheiden.
Het is onduidelijk of geslachtsklieren wegnemen latere mogelijkheden op vruchtbaarheid - via nieuwere technologieën beperkter maakt. De gonaden kunnen mogelijks ei-of spermacellen aanmaken. Vrouwen met ovotesticulair dsd hebben soms ook kleine baarmoeder, afhankelijk van de inwerking van het hormoon AMH.
Als gonaden worden weggenomen of zijn weggenomen in de kindertijd of adolescentie via een gonadectomie moeten er levenslang hormonen (oestrogenen) worden ingenomen. Ook als gonaden niet worden weggenomen, zal extra hormoontherapie worden ingezet. Deze hormonen zullen de puberteitsontwikkeling (zoals borstontwikkeling en vet rond heupen) verder op gang brengen. Ze zijn ook nodig voor behoud van een optimale botsterkte en groei, en voor emotioneel welbevinden. Onderzoek naar de langetermijn effecten van deze hormonen is beperkt.
Sommige meisjes/vrouwen ondervinden neveneffecten van hormoontherapie (stemmingswisselingen, opvliegers ...).
Jongens/mannen
Bij mannen met ovotesticulair dsd heeft het behoud van de gonaden voordelen voor een beetje productie van testosteron, dat in de puberteit voor wat beperkte lichaams- en gezichtsbeharing zal zorgen en groei van de penis. De gonaden kunnen ook wat oestrogenen aanmaken, die kunnen leiden tot borstvorming.
Vaak zullen artsen aanraden om de gonaden, als ze niet zijn ingedaald, vanaf de kindertijd naar de balzak te brengen, zodat ze beter kunnen onderzocht worden (zelf of door artsen via beeldvormingsonderzoek).
Een gonadale biopsie kan door artsen voorgesteld worden als een optie om gonaden die moeilijk echografisch te volgen zijn verder te onderzoeken. Bij een biopsie wordt een klein deel van de gonade(n) onderzocht via een kijkoperatie. Deze operatie houdt ook eigen risico's in, zoals schade aan de gonade(n) en eventueel verlies ervan.
Het is moeilijker om een deeltje van de gonade weg te nemen als er zowel eierstok-als teelbalweefsel in dezelfde gonade aanwezig zijn. Die delen lopen vaak ook in mekaar over, en zijn moeilijk van elkaar te scheiden. Als de gonaden worden weggenomen, worden ze dus vaak volledig weggenomen.
Een extra behandeling met testosteron zal vaak ook voorgesteld worden vanaf de puberteit. Het kan soms de kans op botonkalking verminderen, en zorgt voor meer lichaamsbeharing, een betere spieropbouw, maar ook een verhoogde energie, assertiviteit en meer libido. Veel in beweging blijven en sporten, opname van Vitamine D en Calcium kan ook helpen bij spieropbouw en botontkalking tegengaan.
De penis zal echt niet verder groeien onder invloed van dit testosteron (Callens et al., 2013) . Een testosteronbehandeling in de kindertijd kan bij een kleine penis de groei een beetje versnellen in de kindertijd, maar heeft vaak geen effect op de eindlengte op volwassen leeftijd.
Reeds aanwezige gynaecomastie (borstopzet) wordt door testosteronbehandeling niet verholpen, en kan soms zelfs verergeren.

> Lees hier meer over borstopzet bij mannen en wat er kan gedaan worden
4. BOTSTERKTE
Bij veel mannen en vrouwen met ovotesticulair is er kans op botonkalking (osteoporose). De botsterkte zal dan ook jaarlijks tot tweejaarlijks worden opgevolgd via een botscan.
Een goede afstelling van hormoonmedicatie, veel in beweging blijven en sporten, en opname van Vitamine D en Calcium kan ook helpen om botontkalking tegengaan.
5. PUBERTEIT, ZELFBEELD EN RELATIES
Meisjes met ovotesticulair dsd
De puberteit start meestal niet rond dezelfde leeftijd als bij meisjes zonder ovotesticulair dsd, met borstontwikkeling en vetstapeling ter hoogte van de buik. Dat komt omdat er minder oestrogenen worden geproduceerd. Bij sommige meisjes produceren de gonaden produceren ook wat testosteron, wat kan leiden tot schaam-of okselbeharing en ook wat acne. Meisjes met ovotesticulair krijgen hun maandstonden meestal niet spontaan, omdat er vaak niet zoveel eicellen zijn, hoewel er soms wel een kleine baarmoeder is.
Afhankelijk van hoeveel testosteronsignalen worden aangemaakt en opgepikt, kan de clitoris kan onder invloed van testosteron geproduceerd door de ovotestes in de puberteit eveneens wat verder groeien, omdat het lichaam er gevoelig voor is. Ook de stem kan wat dieper worden of er kan wat extra lichaamshaar komen. Alles hangt af van hoeveel testosteron de gonaden aanmaken.
Sommige meisjes zijn helemaal niet blij met deze veranderingen, en er kan dan overlegd worden met artsen hoe de veranderingen gestopt kunnen worden. Er kan voorgesteld worden om de gonaden, die testosteron produceren, weg te nemen. Of er kunnen puberteitsblokkers worden genomen die de productie van testosteron stoppen.
Andere meisjes zijn echter wel blij met deze veranderingen, vooral als ze twijfelen over hun gevoel meisje of jongen te zijn. Het is niet omdat meisjes een grotere clitoris hebben of meer lichaamshaar, dat ze meer twijfelen aan hun gevoel meisje te zijn. Maar net als vrouwen zonder grote clitoris en veel lichaamshaar, kunnen meisjes en vrouwen met een grotere clitoris en wat meer lichaamshaar het gevoel hebben dat ze op een bepaald ogenblik liever als man door het leven willen.
Sommige van deze lichaamskenmerken kunnen leiden tot heel wat zorgen over 'voldoende of compleet vrouw zijn', vooral in de puberteit. Bij sommige jonge mensen nemen deze zorgen later in de volwassenheid af, omdat ze hun uiterlijk gewoon zijn geworden en de mogelijkheid hebben gehad om positieve relaties en seksuele ervaringen op te doen. Bij andere vrouwen blijven de zorgen, en kunnen gesprekken met een psycholoog verder licht werpen op de redenen. Ook contact met andere meisjes en vrouwen met een gelijkaardige ervaring kan helpen in het praktisch omgaan met de gestelde uitdagingen, zoals beperkte vruchtbaarheid en (lastige) vragen van anderen.
In België is er geen aparte vereniging voor meisjes/vrouwen met ovotesticulair dsd. In Nederland organiseert DSDNederland ontmoetingsmomenten voor mensen met verschillende variaties in sekse-kenmerken.
Neem zeker ook een kijkje op deze pagina, waarbij sommige mensen vertellen over hun ervaringen met vrienden, familie, partners en relaties.
Jongens met ovotesticulair dsd
Bij jongens met ovotesticulair dsd is er vaak een vertraagde puberteit, minder lichaams- en gezichtsbeharing, een minder diepe stem en minder groei van de penis, omdat er niet zoveel testosteron wordt geproduceerd door de teelballen. Soms maken de gonaden ook oestrogenen aan, waardoor er wat borstvorming kan zijn.
Deze lichaamskenmerken kunnen - maar hoeven er niet altijd voor te zorgen- dat jongere mannen met ovotesticulair dsd zich minder goed in hun vel voelen en zich zorgen maken over 'voldoende of compleet man zijn'. Bij sommige jonge mensen nemen deze zorgen later in de volwassenheid af, omdat ze hun uiterlijk gewoon zijn geworden en de mogelijkheid hebben gehad om positieve relaties en seksuele ervaringen op te doen. Bij andere mannen blijven de zorgen, en kunnen gesprekken met een psycholoog verder licht werpen op de redenen. Ook contact met andere mannen met een gelijkaardige ervaring kan helpen in het praktisch omgaan met de gestelde uitdagingen, zoals onvruchtbaarheid en (lastige) commentaren van anderen.
In België is er geen aparte vereniging voor mannen met ovotesticulair dsd. In Nederland organiseert DSDNederland ontmoetingsmomenten voor mensen met verschillende variaties in sekse-kenmerken.
Neem zeker ook een kijkje op deze pagina, waarbij sommige mannen vertellen over hun ervaringen met vrienden, familie, partners en relaties.
6. FERTILITEIT
De vruchtbaarheidsopties zijn erg afhankelijk van de situatie van de gonaden. Toch produceren de ovotestes meestal geen of zeer beperkt zaad-of eicellen, en van lage kwaliteit.
Bij vrouwen met ovotesticulair dsd en een baarmoeder kan die onder invloed van het innemen van oestrogeen wat verder groeien. Vrouwen zouden dan eventueel via eiceldonatie wel zwanger kunnen worden.
In onderzoek wordt ook gezocht naar andere vormen om de vruchtbaarheid van mannen en vrouwen met ovotesticulair dsd te verhogen. Eén van de opties daarbij is het extraheren van stamcellen of zaadcel/eicelvoorlopercellen in de gonaden die dan verder moeten uitrijpen tot sperma en eicellen in het laboratorium. Dit is echter nu nog zeer experimenteel onderzoek en wordt nog niet in de praktijk uitgevoerd.
Extra informatie
Verenigingen
Nederlandstalig (Nederland)
Brochures en websites voor ouders
Nederlands
-
dsdfamilies.org - Als je baby geboren wordt met geslachtsdelen die er anders uitzien
-
cyberpoli.nl -ovotesticulair dsd
Engels
Brochures en websites voor kinderen en jongeren
Engels
dsdteens.org - vanaf 10 jaar en ouder
Brochures voor huisarts
DSDNederland- Informatie voor de huisarts, 46, XY disorders/differences of sex development